在21 CFR第210和211部分中,21 CFR第210部分涉及药品的制造、加工、包装或持有,而21 CFR第211部分涉及成品药品。本cGMP指南涉及制药和药物相关行业。
21 CFR第210和211部分
此举是为了回应人们对当时不符合标准的药品生产做法的担忧。1962年的药物改造为药物制造带来了现代质量保证和控制原则。后来添加了“当前”一词,使其成为“CGMP”(或CGMP),以暗示该法规允许改变技术以实现GMP.
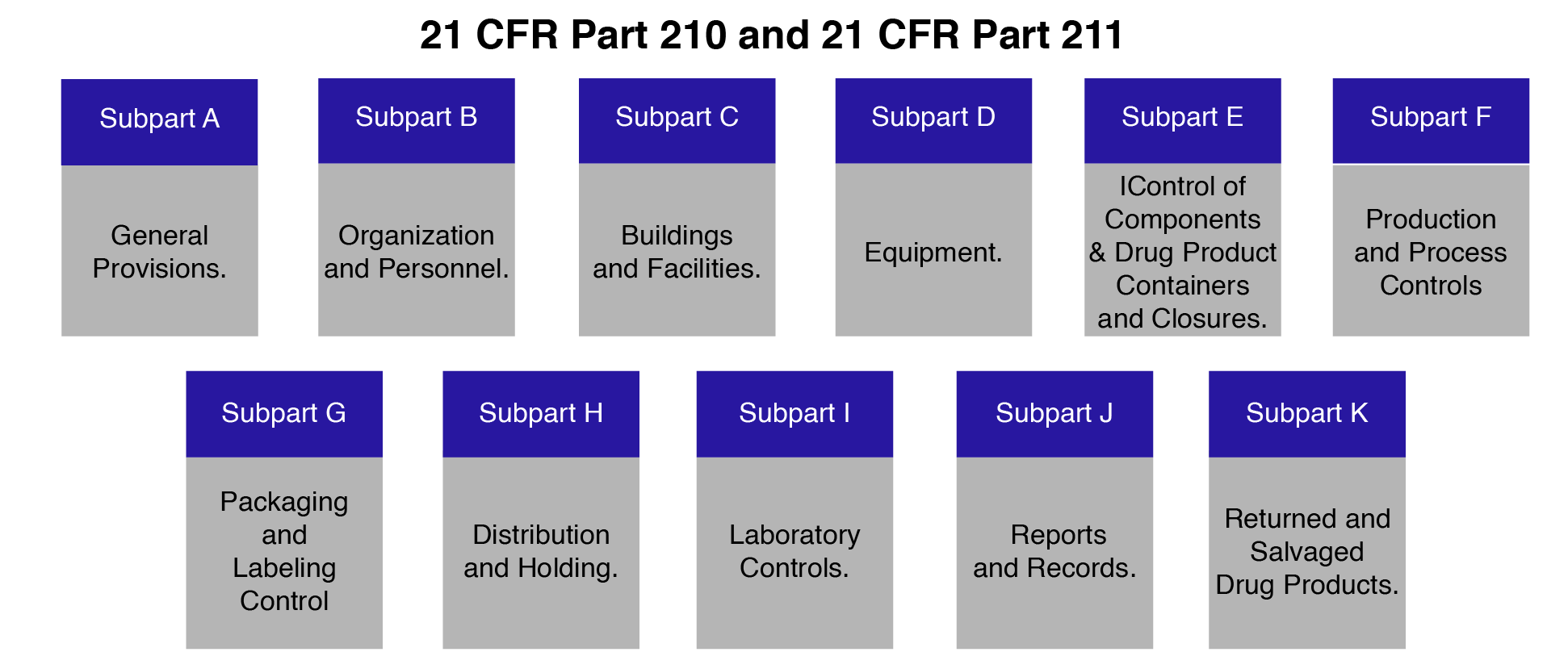
21 CFR第210部分和21 CFR部分211
成品药品的现行良好生产规范
- 子部分A——一般规定。
- 子部分B–组织和人员。
- 子部分C——建筑物和设施。
- 子部分D–设备。
- 子部分E–成分和药品容器及封口的控制。
- 子部分F–生产和过程控制。
- 子部分G–包装和标签控制
- 子部分H–分配和持有。
- 子部分I–实验室控制。
- 第J子部分——报告和记录。
- 子部分K–退回和回收的药品。

